ガイガーは金箔にぶつけたアルファ粒子がたまにあり得ない方向へ散乱することに気づくのです。
さらに研究をすすめると、あろうことか跳ね返ってくる粒子があることも発見されます。

なぜ高いエネルギーを持つアルファ粒子が、薄っぺらい金箔で跳ね返るのか? これは紙の壁に大砲を打ち込んだら、そのまま弾がこちらへ跳ね返されたというくらい衝撃的な現象でした。
ラザフォードはこの原因が原子の構造にあると考えました。
そして、原子の中身が正電荷の大きな核を中心に電子が惑星のように軌道を描いて回っているという原子核モデルを思いつくのです。
アルファ粒子は正電荷の粒子です。アルファ粒子が極稀に跳ね返るのは正電荷の原子核にぶつかったためで、たまに散乱を起こすのは、原子核の周りに浮かぶ電子の極近距離を通って影響を受けたためと考えたのです。
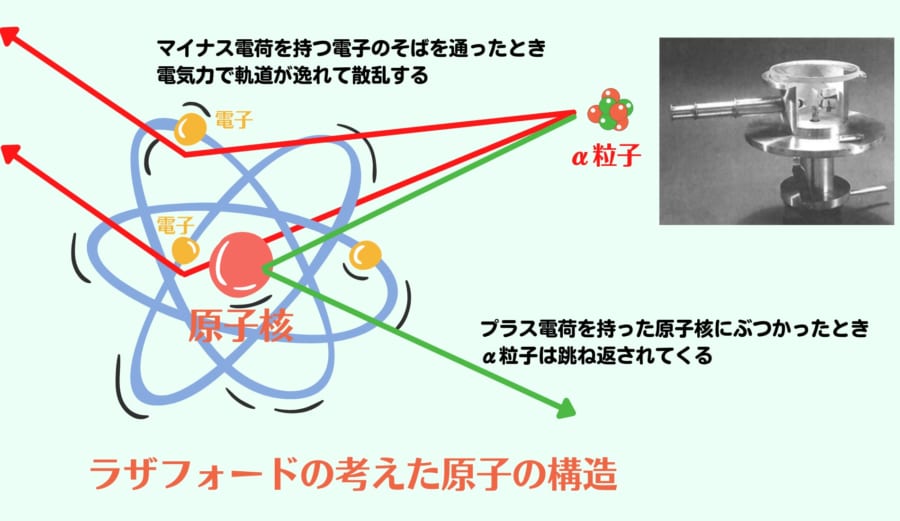
このときラザフォードの考えた原子核モデルは厳密には正しくないのですが、現代の私達が原子を思い浮かべるイメージの原型になりました。
そしてこのモデルは、正確では無いにも関わらず、カッコいいので今でもアメリカ原子力委員会の記章になっています。

正確でないということを強調しましたが、この辺りから物理学は新しく発見された事実を視覚的に表現することが難しくなってくるのです。そしてそれは現代まで続いています。
現代でも、多くの人は原子の構造と言われると上の米原子力委員会の記章を思い浮かべると思いますし、教科書にも上のような図が記載されていたりします。
しかし、このモデルは発表当時は真面目に受け取られませんでした。










































