コロナ感染による場合は、スパイク蛋白抗体に加えてヌクレオカプシド抗体にも染色されるが、この症例では、スパイク蛋白にのみ染色されたので、ワクチン由来の遺伝情報によって産生されたスパイク蛋白と考えられた。
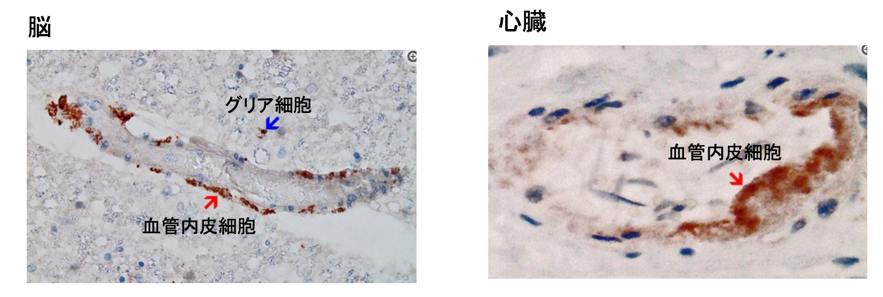
図4 脳、心臓の血管内皮細胞とグリア細胞におけるスパイク蛋白の発現
スパイク蛋白の発現があれば、スパイク蛋白による直接の細胞傷害のほか、抗スパイク蛋白抗体あるいは細胞障害性T細胞による自己免疫機序によって細胞が傷害されてもおかしくない。
ワクチン接種後にみられる心筋炎はスパイク蛋白による心筋傷害と考えられており、ワクチン接種後早期から発症する。壊死性脳炎の原因もスパイク蛋白による傷害と考えれば、心筋炎と同様にワクチン接種後早期から発症すると考えられる。この症例において、脳と心臓の血管内皮細胞にスパイク蛋白が発現し、壊死性脳炎と心筋炎の所見が同時に見られたことは、上記の可能性を支持する。
現在、コロナワクチン接種後のCJDと報告されている症例は、ワクチン接種からの潜伏期間が極めて短いことや、病理検査で異常プリオン蛋白が脳に沈着していることを確認されていないことから、典型的なCJDとは区別した方がよいと思われる。ここでは便宜的にCJD-likeと命名する。この範疇に入る症例については、先入観をもたずにその病因や発症機序を検討する必要があると思われる。
日本で、CJD-likeは発生しているだろうか。3月10日に配布された厚生科学審議会のコロナワクチン接種後の副反応報告にはCJDの病名はない。しかし、意識変容(168例)、意識レベルの低下(687例)、運動機能障害(333例)、刺激に無反応(25例)などCJDを疑う症状が見られた患者は多数報告されている。とりわけ、ワクチン接種後に認知症の症状が急速に進んだ患者の中にはCJD-likeが紛れ込んでいるかもしれない。
ワクチン関連心筋炎の診断に、血中スパイク蛋白の検出が有用であることが報告されているが、同様な発症機序が考えられるCJD-likeの診断においても血中スパイク蛋白の測定が有用かもしれない。
コロナワクチンとCJDとの関係が話題になったのは、もともとスパイク蛋白にプリオン領域が存在するからである。コロナワクチンが典型的なCJDの発症リスクであるかが明らかになるには、今後10年間、20年間にわたる観察を必要とするであろう。










































