ウランは海水中でウラニルイオン(UO₂²⁺)という形でごく微量存在しますが、例えば似た化学的性質を持つバナジウムなど他の金属イオンがはるかに高濃度で含まれており、ウランだけを選択的に「釣り上げる」ことが困難でした。
従来は、ウランに強く結合する特殊な樹脂や繊維(アミドキシム系ポリマーなど)を海水に浸して吸着させる方法が主に試みられ、近年ではこの吸着材の改良によって性能向上とコスト低減が図られてきました。
しかし、それでもウラン1kgを海水から回収するのに数百ドル以上かかるとの報告が多く、実用化のハードルは高いままでした。
こうした中、近年「電気化学的」に海水中のウランを引き離すアプローチも有望視され始めました。
電気の力でイオンを動かしたり化学反応を起こしたりすることで、より速くウランを回収し、吸着材も再利用できる利点があります。
しかし電気化学法にも課題がありました。
海水中でウランイオンを直接回収しようとすると高い電圧が必要になりがちで、エネルギー消費が大きく非効率だったのです。
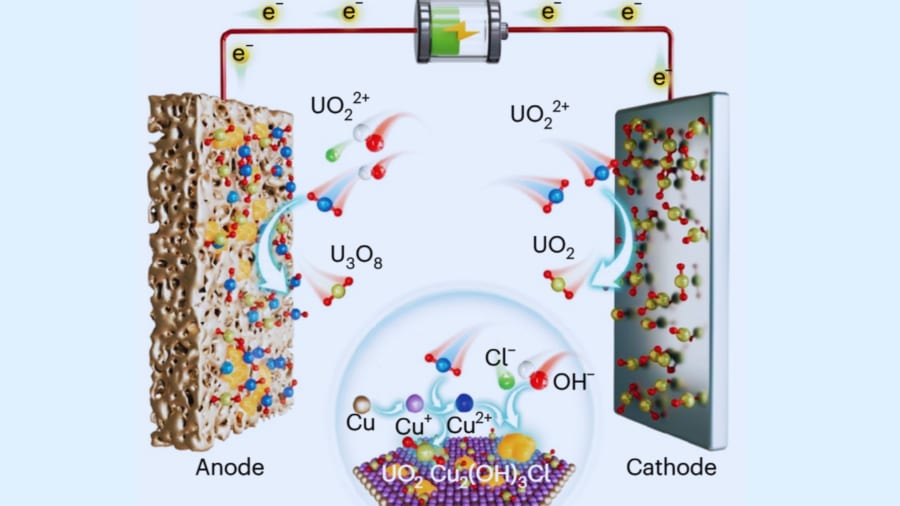
特に、ウランを陰極(マイナス電極)で回収する裏で、陽極(プラス電極)側では水から酸素を発生させる反応などが生じますが、この酸素発生にはかなりの高電圧(1.23V以上)が必要です。
そのため従来型の電気化学的手法では2ボルト以上の電圧を要するケースもあり、結果としてエネルギーコストがかさんでしまいました。
そこで研究チームは、必要電圧を飛躍的に下げてエネルギー効率を高める方法に挑戦しました。
単三電池以下の電力でウランがとれる