特にオリンパス株式会社の研究グループが沖縄に生息する蛍から発見したルシフェラーゼは有望であり、既存の北米産の蛍のルシフェラーゼに比べて4~10倍も明るく黄色の光を発光させることが可能でした。
一方、蛍の発光システムを人工的に再現する研究も進んでおり、理化学研究所では人工基質AkaLumine-HCLと人工酵素Akalucを組み合わせることで、発光効率が従来の100~1000倍で赤く輝く人工生物発光システムAkaBLIを開発しました。
実験にあたってはまず、沖縄の蛍に由来するルシフェラーゼと人工酵素Akalucをそれぞれマウスに組み込んだ系統が作成されました。
たとえで表現するなら、光らせる前準備として、沖縄産の火打石と人工の火打石の設計図を別々のマウスの遺伝子に組み込んだ形となります。
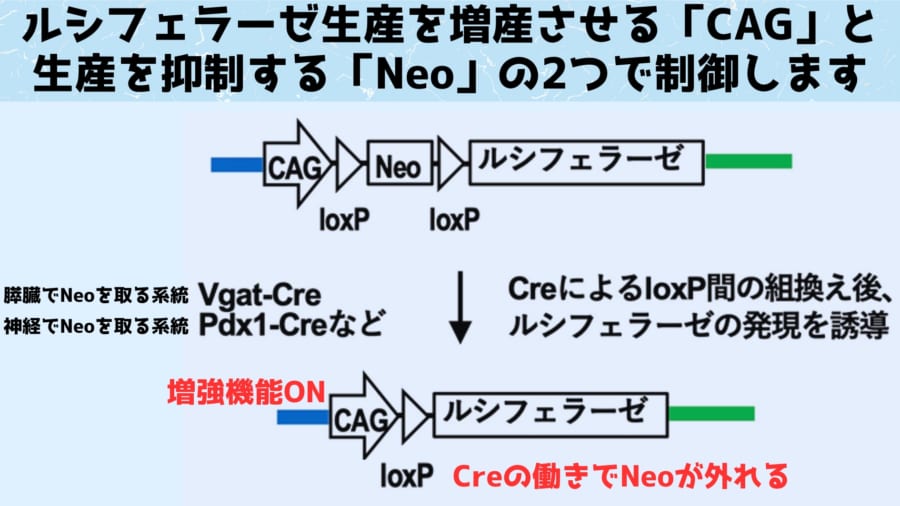
遺伝子を組み込む際には、遺伝子の始まりの部分に抑制装置(Neo)が組み込まれ、上流には、遺伝子発現をブーストする「CAG」と呼ばれる領域(プロモーター)を加えました。 こうすることで酵素の勝手な生産を防ぎつつ、抑制装置(Neo)が外れた場合には強力な活性が得られる状態になります。 そして次に、マウスの体のさまざまな部位で、抑制装置(Neo)を外す仕組み酵素Creを持つマウスと掛け合わせました。 こうすることで、誕生した子マウスたちは、研究者たちが望む臓器でルシフェラーゼやAkaluc(火打石役)が生産されるマウスが誕生します。 / Credit:理化学研究所 . 生体深部を非侵襲的に観察できる多色発光イメージング用マウス 遺伝子操作が終わると、次に研究者たちは発光基質(ロウソク役)であるルシフェリンやAkaLumine-HCLをマウスの体内に注射しました。
マウスたちは暗闇の中でも自分自身から発せられる光で周囲を見ることができます / Credit:Toshiaki Nakashiba et al . Development of two mouse strains conditionally expressing bright luciferases with distinct emission spectra as new tools for in vivo imaging . Lab Animal (2023)