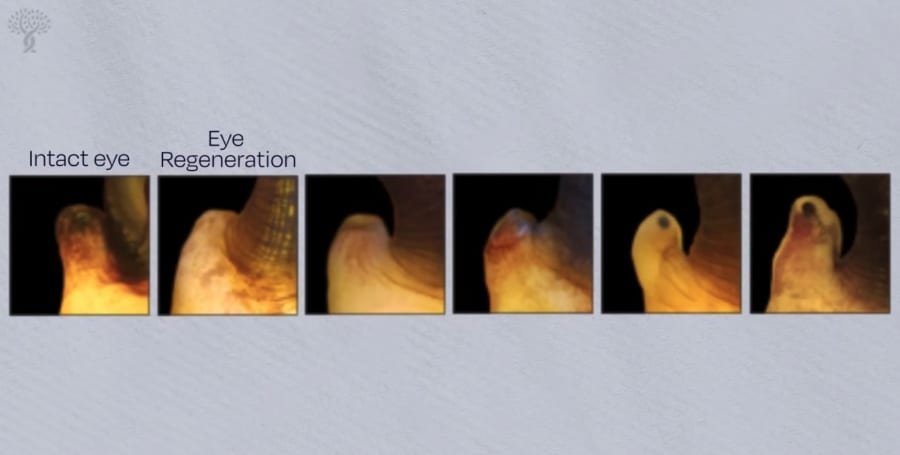
すると、わずか24時間以内に傷口は閉じ、3日目には未分化の細胞からなる“ブラストーマ”が出現。
そこから網膜やレンズが再形成され、28日後には視神経まで含めた完全な眼球構造が再生されていたのです。
しかも、その目は元の目とほぼ同じ構造と遺伝子発現パターンを示していました。
この再生は「エピモルフォーシス」と呼ばれる、細胞分裂と組織再構築を伴うメカニズムで進行しており、これは一部のサンショウウオやゼブラフィッシュが持つ再生能力に近いものです。
スクミリンゴガイのような巻貝に、これほど複雑な器官を再生できる仕組みがあったとは、科学者たちにとっても大きな驚きでした。
人間の目の再生に応用できるか?鍵を握る「pax6遺伝子」
再生のカギを握るのは「遺伝子」です。
チームは、スクミリンゴガイの眼球再生過程でどの遺伝子が活性化されているかを解析しました。
その結果、驚くべきことに、ヒトやマウスなど脊椎動物の眼の発生に関わる「pax6(パックスシックス)」という遺伝子が、巻貝の目の再生時にも活発に働いていることが判明したのです。
しかもpax6遺伝子がなければ、目がまったく形成されないことも、CRISPR-Cas9による遺伝子編集で証明されました。
pax6は、脳や目の形成において極めて重要な遺伝子で、ヒトを含む多くの動物で共通して機能しています。
今回の研究では、この遺伝子が再生過程でも中心的な役割を果たしていることがわかり、「再生医療」の文脈でも注目が集まっています。
チームはさらに、スクミリンゴガイの卵を外部で培養し、mRNAを注入して遺伝子発現を操作する技術も確立しました。
これはスクミリンゴガイが「遺伝子操作可能な再生モデル」として本格的に活用できることを意味します。











































