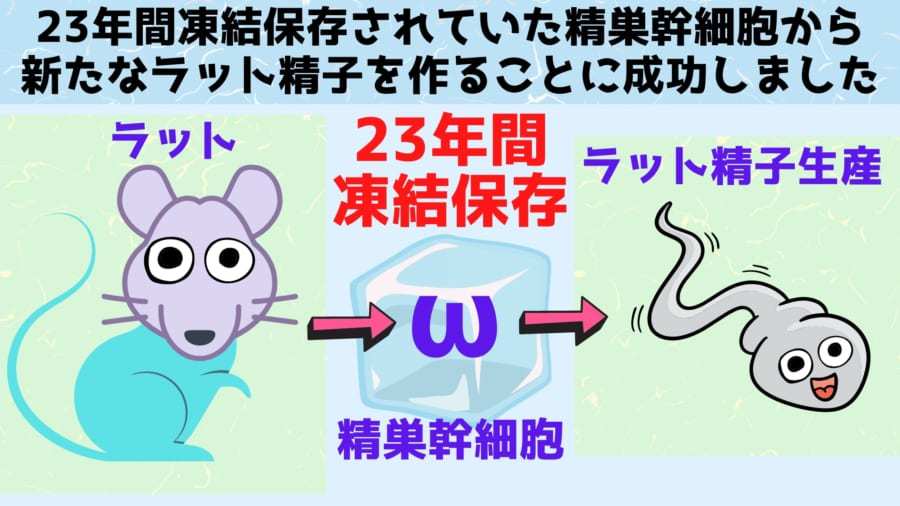
23年間凍っていた「精巣」からても精子は作れるようです。
米国ペンシルベニア大学(UPenn)で行われた研究によれば、23年間凍結状態にあったラットの精巣幹細胞をマウスに移植したところ、完全な形をした精子が生産された、とのこと。
平均的なラットの寿命が2年ちょっとであることを考えると、精巣幹細胞は本体の寿命の10倍もの年月を凍ったまま生き延び、新たな精子を作ったことになります。
この技術が人間にも応用できれば思春期前の段階で、がん治療が必要となった男児にとって、自分の生物学的な子孫を残すことが可能になるかもしれません。
しかし、長期凍結保存によって精子生産能力に支障はなかったのでしょうか?
研究内容の詳細は2022年5月10日に『PLOS BYOLOGY』にて公開されています。
23年間凍っていた精巣幹細胞を解凍したらまだ精子生産能力があったと判明!
精液の凍結保存は古くから行われており、1952年には凍結した牛の精子を使って仔牛が生れたことが報告されています。
人間においても凍結した精子には受精能力があることが知られており、不妊治療や優秀な男性の遺伝子を望む女性に対して、凍結状態の精子を提供するビジネスも存在しています。
この精子凍結は、がん治療を控えた男性たちにとっても子どもを残す手段として救いとなっています。
現在の抗がん剤の多くは精巣の機能に大きなダメージを与え、精子を生産する能力を奪ってしまうことがあるのです。
ただ問題は、小児がんなどによって、思春期前にがん治療を行わなければならなくなった男児にとっては、この方法が利用できないことでした。
なぜなら思春期前の男児たちの睾丸には、冷凍保存すべき精子がまだ存在していないからです。
そこで近年になって着目されるようになったのが、将来精子を作るようになる精巣幹細胞の保存です。
精巣幹細胞とは、いわば「精子のモト」となる細胞であり、精子をはじめ生殖器のあらゆる細胞に変化する能力を持っていることが知られています。
この「精子のモト」を凍結保存することができれば、幼い段階でがん治療を受けた男児でも、大人になって解凍・培養することで、精子を作れるようになるのです。
ただその場合問題となるのは、長期凍結保存が与える影響です。
精子の場合、比較的長期にわたって凍結保存できることが知られています。
例えば牛の場合では、15年間凍結状態にあった精子から仔牛が生れたことが報告されています。
しかし「精子のモト」となる精巣幹細胞にもそのような長期保存が可能であるかは、十分に検証ができていませんでした。
(※ある程度の万能性をもった幹細胞は、遺伝子運搬マシーンである精子とは大きく異なる存在です。ある意味では精子よりも受精卵に近いと言えるでしょう)
そこで今回、ペンシルベニア大学の研究者たちは研究室で23年間凍結状態にあったラットの精巣幹細胞を、免疫力を奪ったマウスに移植し、正常な精子が作られるかを確かめることにしました。
結果、ラットの精巣幹細胞は分裂と増殖を繰り返し、マウス体内で完全に分化した精子が生産されていることが判明します。
つまりラットの精巣幹細胞は本体寿命の10倍に及ぶ凍結期間を、精子生産能力を保持したまま生き延びていたのです。
しかし全く問題なしとはいきませんでした。
23年間氷漬けにされた精巣幹細胞には、短期間凍結ではみられない変化が起きていたのです。
長期凍結は細胞機能を劣化させていた

長期凍結の影響は、解凍後の細胞の遺伝子発現パターンに既に現れていました。
研究では比較対象として、凍結されていない新鮮な精巣幹細胞と短期間(数カ月)の凍結を受けた精巣幹細胞が用意され、長期凍結後の精巣幹細胞とともに遺伝子の発現パターンが調べられました。
すると、凍結期間にかかわらず「凍結という現象」によって影響を受ける遺伝子がいくつか存在することが判明します。
細胞が凍結すると氷の結晶が発生し、細胞内に存在する様々なシステム基盤を引き裂いてしまいます。
これらの物理的な傷害が引き起こす影響は短期凍結でも長期凍結でも、凍結があった時点で同じように発生すると考えられます。
一方で、短期凍結に比べて長期凍結のほうが、より大きな遺伝子発現パターンの違いがあることも判明しました。
この結果は、凍結時間の長さが遺伝子活性に何らかの影響を与えていることを示します。
また解凍した精巣幹細胞をマウスの精巣に移植した後にも変化がありました。
長期凍結を受けていた細胞は短期凍結に比べて、細胞コロニーの形成能力が大きく落ちていました。
種をまたいで移植された細胞は通常、移植先でコロニーと呼ばれるまとまった状態に移行するはずなのですが、長期凍結を受けた精巣幹細胞では形成されるコロニー数がかなり少なくなっていたのです。
またコロニーが形成されたとしても、生産される精子の量は凍結を受けていない新鮮な細胞や短期凍結を受けた細胞に比べて3分の1になっていました。
研究者たちが原因を調べたところ、長期凍結を受けた精巣幹細胞は単に死んでいたのではなく、未分化細胞(精子のモトの状態)が大幅に多くなっていたことが判明します。
さらに興味深いことに、この未分化状態の細胞は自己複製を繰り返す傾向がありました。
つまり凍結は遺伝子の発現パターンに時間に依存する変化を与えるだけでなく、精巣幹細胞をより万能状態に押しとどめ、精巣幹細胞から精子が作られる速度も低下させていたのです。
この結果は、長期間の凍結が精巣幹細胞としてのアイデンティティーや機能を劣化させていることを示します。
幹細胞の長期保存技術は「ほぼ不老」への最短経路
今回の研究により、23年にもおよぶ長期凍結状態にあった精巣幹細胞にも、精子を新たに生産する能力が残っていることが示されました。
研究者たちはマウスの精巣からラットの精子を上手く取り出すことができれば、ラット卵子を受精させられると述べています。
同様の仕組みが人間でも機能すれば、凍結保存されていた精巣幹細胞を、がんの完治後に自分の精巣に戻すことで、精子生産能力を復活させられるでしょう。
一方で、長期間の凍結は精巣幹細胞のアイデンティティーを曖昧にし、精子の生産速度を大幅に減らすことも明らかになりました。
これらの悪影響を減らす方法として研究者たちは、定期的に細胞の状態を調査し、悪影響が少ない細胞を選択して培養し、再凍結することが重要であると述べています。
もし体の各部位の幹細胞を安定的に長期凍結保存できるようになれば、保存された幹細胞から定期的に一部を取り出し培養して自分の体に入れることで、いつまでも若い体を維持できるようになるでしょう。
(※若返りの限度は幹細胞を保存した年齢に依存します)
これらの手順には莫大な費用がかかりますが、実現できれば理論上「ほぼ不老」状態を手にする最短経路となるでしょう。
参考文献
Frozen Testicular Tissue Can Be Reimplanted After 20 Years and Go On To Make Viable Sperm
元論文
Reestablishment of spermatogenesis after more than 20 years of cryopreservation of rat spermatogonial stem cells reveals an important impact in differentiation capacity
提供元・ナゾロジー
【関連記事】
・ウミウシに「セルフ斬首と胴体再生」の新行動を発見 生首から心臓まで再生できる(日本)
・人間に必要な「1日の水分量」は、他の霊長類の半分だと判明! 森からの脱出に成功した要因か
・深海の微生物は「自然に起こる水分解」からエネルギーを得ていた?! エイリアン発見につながる研究結果
・「生体工学網膜」が失明治療に革命を起こす?
・人工培養脳を「乳児の脳」まで生育することに成功













































